|
Độ hòa tanĐộ hòa tan là một đặc điểm hòa tan của chất rắn, chất lỏng hoặc chất khí vào dung môi để tạo ra một dung dịch đồng nhất. Độ hòa tan của một chất phụ thuộc chủ yếu vào các tính chất vật lý và hóa học của chất tan và dung môi cũng như nhiệt độ, áp suất và pH của dung dịch. Hiếu theo nghĩa rộng hơn độ hòa tan của một chất trong một dung môi nhất định được đo đạc bằng nồng độ bão hòa, bão hòa ở đây có nghĩa là việc thêm nhiều chất tan sẽ không làm tăng nồng độ của dung dịch và bắt đầu xuất hiện kết tủa của một lượng chất tan dư. Yếu tố ảnh hưởng đến độ hòa tanNhiệt độ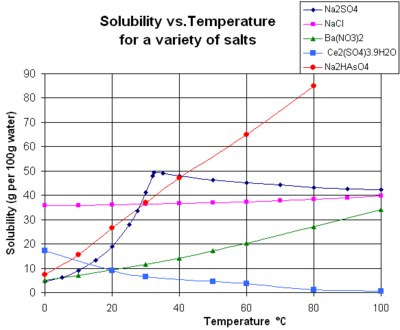 Chất khí hòa tan thể hiện những ứng xử phức tạp hơn theo nhiệt độ. Khi nhiệt độ tăng, khí thường trở nên ít hòa tan trong nước ( đến tối thiểu, dưới 120°C cho hầu hết các khí phổ biến[1]), nhưng hòa tan nhiều hơn trong các dung môi hữu cơ.[2] Đồ thị thể hiện các đường cong hòa tan của một số muối vơ cơ ở dạng rắn (nhiệt độ tính theo độ Celsius).[3] Độ hòa tan của các hợp chất vô cơ gần như luôn tăng theo nhiệt độ. phụ thuộc vào độ hòa tan khác nhau của các chất tan trong các dung môi nóng và lạnh. Áp suấtĐối với các pha nén (rắn và lỏng), sự phụ thuộc vào áp suất của độ hoà tan đặc biệt yếu và thường bị bỏ qua trong thực tế. Giả thiết một dung môi lý tưởng, sự phụ thuộc có thể xác định theo:với i là các nhân tố thành phần, Ni là tỷ lệ mol của thành phần thứ ith trong dung dịch, P là áp suất, T là hằng số nhiệt độ, Vi,aq là thể tích mol riêng phần của phần tử thứ i trong dung dịch, Vi,cr là thể tích mol riêng phần của phần tử thứ ith trong chất rắn hòa tan, và R là hằng số khí lý tưởng.[4] Sự phụ thuộc áp suất của độ hòa tan thỉnh thoảng có ý nghĩa thiết thực. Ví dụ, sự nhiễm bẩn lắng đọng calci sulfat trong các mỏ và giếng dầu (làm giảm độ hòa tan của nó khi giảm áp suất) có thể làm giảm khả năng khai thác theo thời gian. Tham khảo
|