|
Zeolit Zeolity (řecky zein – „vařit“ a lithos – „kámen“) jsou hlinitokřemičité minerály mající mikroporézní strukturu. Termín zeolit byl původně vytvořen v 18. století švédským mineralogem Axelem Fredrikem Cronstedtem, který pozoroval, že při rychlém ohřívání přírodních minerálů kameny začnou tančit. Použitím řeckých slov, které znamenají „kameny, které vaří“, pojmenoval tento materiál zeolit. Kameny „vřou“, protože voda obsažená v pórech zeolitu uniká při zahřívání ven. Zeolity jsou krystalické hydratované alumosilikáty alkalických kovů a kovů alkalických zemin. Jedinečnost spočívá v tom, že prostorové uspořádání atomů vytváří kanálky a dutiny konstantních rozměrů. V těchto kanálcích se mohou zachytávat látky tuhého, kapalného a plynného skupenství. 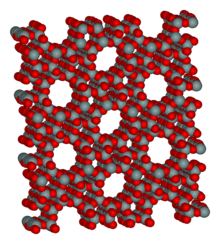 VznikZeolity jsou podstatnou složkou vulkanických tufů a vulkanoklastických sedimentů, které vznikají reakcí vulkanických skel a vody v sedimentačních bazénech. Vznikají též reakcí vulkanických skel s prosakující meteorickou vodou, kde mohou vzniknout ložiska mocná až několik stovek metrů. Zeolity jsou také masivně zastoupeny v hlubokooceánských sedimentech. Mineralogické ukázky zeolitů nalezneme převážně v nízce metamorfovaných horninách a zejména v alterovaných vulkanitech (výplně v podobě mandlí, dutinek – často sbírkové kusy zeolitů). Zeolity zde krystalovaly v rámci nízkoteplotní hydrotermální mineralizace a v ČR je lze nejčastěji nalézt v neovulkanitech Českého středohoří a Doupovských hor.[1] Vlastnosti Stejně jako všechny tektosilikáty mají zeolity trojrozměrnou vazbu tetraedrů SiO4 a AlO4, které jsou navzájem propojené sdílením vrcholových kyslíků. Negativní náboj na mřížce zeolitů vyrovnávají kationty, které obsazují mřížkové dutiny. Nejdůležitějším strukturním rozdílem mezi zeolity a ostatními tektosilikáty jsou větší rozměry mřížkových dutin a jejich vzájemné propojení kanály. Molekulová voda i jiné látky mohou vstupovat do struktury zeolitů a opět se uvolňovat bez poškození původní mřížky. Tato vlastnost se samozřejmě odráží na mřížkových parametrech, které jsou u zeolitů velmi proměnlivé. Při zahřívání je zeolitová voda snadno vypuzována ze struktury a bezvodý materiál může absorbovat jiné molekuly, které nejsou větší než kanály, kterými musí projít. Tato specifická schopnost struktur zeolitů umožňuje jejich využití jako molekulárního síta. Zeolity jsou navzájem odlišné různým sestavením tetraedrů v rámci trojrozměrné sítě a také velikostí a tvarem výsledných kanálů. Základní konfigurace jsou smyčky 4, 5, 6, 8, 10 a 12 tetraedrů. Vzájemně propojené smyčky utvářejí větší a komplikovanější polyedrické klece. V chemickém složení zeolitů dominuje křemík a hliník, přičemž Al nikdy nepřevažuje nad Si. V závislosti na jejich poměru v tetraedrických pozicích jsou obsazeny dutiny ionty Na, Ca, K a Ba.[1]
VyužitíZeolity mají díky své jedinečné struktuře široké využití. V přírodě bylo popsáno více než 40 různých minerálů této skupiny a synteticky bylo připraveno nejméně 100 zeolitů pro průmyslové a komerční využití.[3] Úprava pitné vodyZeolity se díky svým vlastnostem, jako jsou adsorbce těžkých kovů nebo amoniaku, využívají po celém světě k úpravě pitné, odpadní, bazénové a surové vody. Filtrace bazénůFyzikální vlastnosti zeolitu se výrazně od sebe liší a je nutné vždy používat při úpravě vody vhodný typ zeolitu. Pro úpravu vody v bazénu, kde se standardně používají rychlé filtry cca 40-50m3/Hod je nutné používat zeolity s co nejvyšší tvrdostí ( 7 Mohs ) a menší velikostí pórů. Nejvyšších tvrdostí s nano póry dosahují pouze zeolity z oblasti Austrálie, kde se tvrdost zeolitů pohybuje okolo 6 - 7 Mohsové stupnice tvrdosti. Běžné zeolity, které jsou těžené v Evropě, USA nebo ASII dosahují tvrdosti pouze 2-3 Mohsovy stupnice tvrdosti s makro póry, které nejsou vhodné pro rychlé diskontinuální filtrace. Australský typ zeolitů mají velikost pórů okolo 50 nm a jsou proto považovány jako antibakteriální. Zeolity jsou využívány při úpravě bazénové vody hlavně kvůli iontové výměně, kdy dochází k adsorbci amoniaku z vody, kam se dostal z lidské pokožky a v reakci s chlorem, který je používán k desinfekci dochází k reakci při vzniku anorganických chloraminů – monochloramin (NH2Cl), dichloramin (NHCl2) a trichloramin (NCl3).[4] DomácnostZeolity bývají jednou ze základních složek bezfosfátových pracích prášků.  ŠperkařstvíNejvzácnějším minerálem ze skupiny zeolitů je thomsonit. Má významný šperkařský potenciál a je pro tyto účely vyhledáván na lokalitě Hořejší jezero v Minnesotě, USA. Zde dochází k uvolňování nodulí, které erodují z bazaltů a následně jsou vyplavovány na tamějších plážích (dokonce jsou sbírány potápěči v hlubších partiích jezera). Tyto nodule mají velice překrásnou páskovanou strukturu, kde se střídají barvy černé, oranžové, červené, žluté, růžové až fialové. Tyto barvy jsou způsobeny vlivem nečistot, které se navázaly do struktury zeolitu a nejčastěji se zde vyskytuje plno mědi, která může vytvářet až samostatné měděné inkluze, kterým se říká "měděné oči". Při vyleštění se zde může objevit jev chatoyance, též známý jako "efekt kočičího oka". Chemický průmyslFyzikálně-chemické vlastnosti zeolitu vyplývají z jeho alumosilikátové kostrovité struktury, která umožňuje dehydrataci, výměnu iontů a absorpci molekul různé velikosti, aniž by došlo k jejich narušení. To umožňuje používat zeolit jako sorbent, molekulární síto a katalyzátor. ZemědělstvíPřidáním zeolitu do půdy můžeme významně ovlivnit některé z půdních vlastností. Obohacuje půdu o stopové a biogenní prvky. Příznivě působí na růst a vývoj plodin, zlepšuje úrodnost a zvyšuje výnos pěstovaných plodin. Lépe provzdušňuje půdní komplex. U písčitých zvyšuje úrodnost, lépe zadržuje vodu a postupně ji uvolňuje dle potřeb rostlin. MedicínaDíky velkému povrchu, jež má tento minerál k dispozici, se užívají přípravky, které jsou vyrobeny na bázi zeolitu. Významné využití ve zdravotnictví je v tom, že tyto přípravky jsou schopny stavět krvácení. Při kontaktu s krví v ráně a jejím okolí vychytávají z krve molekuly vody, zatímco větší struktury zůstanou v ráně a tím podpoří přirozené stavění krvácení. Druhou velmi významnou aplikací je použití v kyslíkových koncentrátorech, kde jsou umělé zeolity schopné za určitého tlaku odfiltrovat dusík ze vzduchu, takže prošlá směs má výrazně vyšší podíl kyslíku. Filtr je ovšem následně nutné regenerovat (profouknout zpět za nižšího tlaku), čas regenerace se řídí velikostí filtru, řádově jsou to desítky sekund. Přístroje mají proto alespoň dva filtry, které pracují střídavě. AkvaristikaZeolit se používá jako filtrační medium pro čištění zahradních jezírek, rybníků a akvárií. Pórovitá struktura zeolitu poskytuje optimální povrch pro kolonizaci biologicky užitečných nitrifikačních bakterií. Ohřev a ochlazováníZeolity se používají jako solární termokolektory a v adsorpčních chladicích zařízeních. V těchto aplikacích se využívá jejich vysoké zahřívání při adsorpci a schopnost hydratace a dehydratace při zachování strukturální stability. Tato hygroskopická vlastnost spojená s inherentní exotermní reakcí (způsobující zahřátí) při přechodu z dehydratované do hydratované formy předurčuje přírodní zeolity k využití odpadového tepla a tepelné sluneční energie. VýskytZeolity můžeme rozdělit do dvou skupin. Zeolity vytvořené uměle a přírodní zeolity. Díky efektivní výrobě průmyslových zeolitů, mají oproti těm přírodním téměř nulový výskyt nečistot v mřížkách. Dá se tedy sestavit dokonalá molekula, která se v přírodě běžně nevyskytuje a má lepší vlastnosti. Přírodní zeolityTyto zeolity se dobývají většinou povrchovou metodou lomu. Nadloží je odstraněno, aby umožnilo přístup k rudě a následně mohla být odstřelena nebo roztrhána pomocí těžké techniky. Při zpracování se ruda drtí, suší a mele. V současné době je roční světová produkce přírodního zeolitu asi 3 miliony tun. Hlavními producenty v roce 2010 byla Čína (2 milionů tun), Jižní Korea (210 000 tun), Japonsko (150 000 tun), Jordánsko (140 000 tun), Turecko (100 000 tun), Slovensko (85 000 tun) a Spojené státy americké (59 000 tun).[5] Díky dobré dostupnosti materiálu a malých nákladů na jeho těžbu, jsou přírodní zeolity stále rentabilní a jejich těžba má do budoucna veliký potenciál. Umělé zeolityExistuje zde několik druhů syntetických zeolitů, které využívají proces pomalé krystalizace gelu oxidu křemičitého a oxidu hlinitého v přítomnosti alkálií a organického templátu. Klíčovým krokem při syntéze zeolitů je sol-gel hydrolýza, která může do struktury zabudovat kovy nebo oxidy kovů. Konečné vlastnosti syntetického zeolitu jsou tak závislé na složení reakční směsi, pH reakčního prostředí, reakční teplotě a času a také na povaze použitého templátu. Tyto zeolity jsou velmi stabilní a mají dobré vlastnosti, které můžeme upravovat přimícháváním různých látek do struktury a následně tak upravovat materiál podle potřeby užití. Jejich struktura oproti přírodním analogům je přesněji definovaná a pravidelnější. Rozdělení zeolitůZeolitová skupina dle Nickel-Strunzovy klasifikace zahrnuje:[2][3][6]
GalerieReference
Externí odkazy
|











