|
การผลิตไฮโดรเจนการผลิตไฮโดรเจน เป็นกระบวนการสร้างไฮโดรเจนจากสารเคมีอื่น เทคโนโลยีการผลิตที่ใช้กันอย่างแพร่หลายในปัจจุบันคือการนำสารไฮโดรคาร์บอนมาทำการเปลี่ยนแปลงโครงสร้างโมเลกุลด้วยไอน้ำ (steam reforming) นอกจากนั้นก็ยังมีวิธีการแยกสลายสารที่อยู่ในสถานะของเหลวด้วยไฟฟ้า (electrolysis) และ การแยกสลายสารด้วยความร้อน(thermolysis)
Steam reforming พลังงานจากซากดึกดำบรรพ์ เป็นแหล่งผลิตหลักของอุตสาหกรรมไฮโดรเจน จากแก๊สธรรมชาติด้วยประสิทธิภาพ 80% หรือจากสารไฮโดรคาร์บอนอื่นด้วยประสิทธิภาพแตกต่างกันไป ขั้นตอนแรก ไอน้ำ (H2O) ที่อุณหภูมิ 700-1100°C ทำปฏิกิริยาดูดความร้อนกับมีเทน (CH4) จะได้ซินแก๊ส(syngas) ตามสูตร
ขั้นตอนที่สอง ปฏิกิริยาคายความร้อนที่เรียกว่า water gas shift reaction จะเกิดขึ้นที่อุณหภูมิ ต่ำลงประมาณ 130°C จะได้ไฮโดรเจนเพิ่มชึ้น
จำเป็นอย่างยิ่งที่จะต้องใส่น้ำ(ไอน้ำ)เข้าไป อะตอมของอ๊อกซิเจน (O) จะถูกดึงออกจากน้ำ ไปทำปฏิกิริยาอ๊อกซิเดชั่นกับ CO ได้ CO2 เกิดความร้อนทำให้ขบวนการดำเนินต่อไป ความร้อนที่ต้องการขับเคลื่อนขบวนการนี้ทั่วไปแล้วได้มาจากการเผาบางส่วนของมีเทน ===การแยกเอา CO2 ออก ขบวนการนี้ จะได้ CO2 ออกมาด้วย ถ้าโรงผลิตนี้ ผลิตแต่ไฮโดรเจนอย่างเดียว วิธีกำจัด CO2 โดยไม่ให้มีผลกระทบกับสิ่งแวดล้อม สามารถทำได้โดยการฉีดมันเข้าไปในถังเก็บน้ำมันหรือแก๊ส วิธีผลิตอื่นๆจากซากดึกดำบรรพ์
เราจะใช้ TPOX หรือ CPOX ขึ้นอยู่กับสารซัลเฟอร์ในเชื้อเพลิงที่นำมาใช้ CPOX จะถูกใช้เมื่อ ปริมาณซัลเฟอร์ต่ำกว่า 50 ppm แต่จากการค้นคว้าเร็วๆนี้ CPOX สามารถใช้กับปริมาณซัลเฟอร์ได้ถึง 400 ppm
ผลิตจากน้ำขบวนการแยกไฮโดรเจนจากน้ำด้วยไฟฟ้า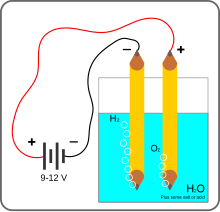 แบ่งออกเป็น 3 แบบใหญ่ๆตามชนิดของเซลล์คือ solid oxide electrolysis cells (SOEC's), polymer electrolyte membrane cells (PEM) and alkaline electrolysis cells (AEC's). SOEC ทำงานที่อุณหภูมิสูง ราว 800°C. PEM electrolysis cells ทำงานที่อุณหภูมิต่ำกว่า 100°C ซึ่งง่ายที่สุด ส่วน AEC ใช้ KOH(potassium carbonate) ชนิดเข้มข้นเป็น electrolyte และทำงานที่อุณหภูมิสูงถึง 200 °C. ขบวนการแยกไฮโดรเจนจากน้ำด้วยไฟฟ้าน้ำจะแตกตัวได้เองที่อุณหภูมิ 2500 C ซึ่งการผลิตวิธีนี้ใช้อุณหภูมิสูงเกินกว่าระบบท่อและอุปกรณ์จะรับได้ ต้องใช้ตัวช่วยเพื่อให้อุณหภูมิลดลงมา ขบวนการแยกไฮโดรเจนจากน้ำด้วย photobiological เป็นการใช้สาหร่ายผลิตไฮโดรเจน ในขบวนการสังเคราะห์แสงของสาหร่าย ถ้าขาดซัลเฟอร์ มันจะผลิตไฮโดรเจนออกมา แทนที่จะเป็นอ๊อกซิเจน อัตราการเปลี่ยนแสงจากดวงอาทิตย์ให้เป็นไฮโดรเจนก็จะสูงกว่า 10 เปอร์เซนต์ โดยผลิตได้ถึง 12 cc ต่อ ชม. ขบวนการแยกไฮโดรเจนจากน้ำด้วย photocatalyticเหมือนการแยกน้ำด้วยไฟฟ้า แต่ใช้ตัว photocatalyst แขวนไว้ในน้ำ แทนที่จะใช้ photovoltaic ซึ่งทำให้มีประสิทธิภาพเพิ่มขึ้น Sulfur-iodine cycleเป็นขบวนการทางเคมีที่มีประสิทธิภาพในการแยกไฮโดรเจนออกจากน้ำได้ดีกว่ามากๆ ซัลเฟอร์และไอโอดีนสามารถนำกลับมาใช้ใหม่ได้ และไม่ใช่วัสดุสิ้นเปลือง เหมาะกับการผลิตไฮโดรเจนด้วยอุณหภูมิสูงจากเตาปฏิกรนิวเคลียร์หรือระบบผลิตพลังแสงอาทิตย์เข้มข้น concentrating solar power systems (CSP) Biohydrogen routesมวลชีวภาพและเชื้อเพลิงขยะ สามารถนำมาผลิตไฮโดรเจนได้ ด้วยวิธีการแปรสภาพเป็นแก๊ส การหมักการหมักเป็นการเปลี่ยนสารอินทรีย์ให้เป็นแก็สไฮโดรเจนชีวภาพโดยใช้แบคทีเรียที่มีระบบการย่อยหลายๆอย่างทั้งแบบใช้แสงและแบบไม่ใช้แสง เช่นแบคทีเรียแบบใช้แสง ชื่อ Rhodobacter sphaeroides SH2C สามารถเปลี่ยนโมเลกุลของกรดไขมันเล็กๆให้เป็นไฮโดรเจนได้ Synthetic biology Biocatalysed electrolysisนอกเหนือจากการหมักแบบมืด ก็คือ electrohydrogenesis (การแยกน้ำด้วยไฟฟ้าโดยการใช้จุลินทรีย์) การใช้เซลล์เชื้อเพลิงจุลินทรีย์ ทำให้น้ำเสียหรือซากพืชต่างๆสามารถถูกนำมาใช้ผลิตพลังงานได้ Biocatalysed electrolysis ไม่เหมือน biological electrolysis เพราะ biological ทำให้สาหร่ายผลิตไฮโดรเจนได้ทันที แต่ biocatalysed electrolysis จะผลิตไฮโดรเจนได้โดยต้องผ่านเซลล์เชื้อเพลิงจุลินทรีย์ก่อน ขบวนการนี้ใช้ได้กับพืชน้ำเช่น ต้นกก หญ้าหวาน cordgrass ข้าว มะเขือเทศ lupines และสาหร่าย เป็นต้น ไฮโดรเจนหมุนเวียนปัจจุบัน สามารถผลิตไฮโดรเจนได้จากพลังงานหมุนเวียน เช่นใช้แก๊สจากการฝังกลบขยะ หรือใช้ไฟฟ้าจากพลังงานหมุนเวียนเพื่อผลิตไฮโดรเจนโดยการแยกจากน้ำ เป็นต้น อ้างอิงวิกิมีเดียคอมมอนส์มีสื่อที่เกี่ยวข้องกับ การผลิตไฮโดรเจน |