|
悪性リンパ腫悪性リンパ腫(あくせいリンパしゅ、英語: Malignant Lymphoma、略称:ML)は、血液のがんで、リンパ系組織から発生する悪性腫瘍である。 概説リンパ系組織は全身を巡っているため、肉腫及び癌腫の癌とは異なり、外科手術による切除は行わず(ただし、腫大による圧迫などを緩和するため姑息手術を行うことはある)、主に放射線療法および化学療法を適応する。リンパ腫には「良性」はないため、必ず「悪性」ということになる。日本語の病名としては明示的に「悪性リンパ腫」と呼び習わしている。該当診療科目は血液内科や耳鼻咽喉科、また診断および治療の観点から放射線科とチーム医療を踏まえた範囲となる。 悪性リンパ腫は、単一ではなく、多様な病型のリンパ系組織のがんの総称である(その疾患分類については今でも分類作業が進行中である)。病型を大別すると、ホジキンリンパ腫 (Hodgkin's lymphoma, HL、あるいはHodgkin's disease, HD) と非ホジキンリンパ腫 (non Hodgkin's lymphoma, NHL) がある。欧米ではホジキンリンパ腫が多数を占めるが、日本人のホジキンリンパ腫は約10%であり、日本では殆どが非ホジキンリンパ腫で占めている。病型によって治療方針および予後が大きく異なるので、リンパ腫では自己の病型を知ることが重要である。 リンパ腫は全身に発生するというその性質上、治療を行ってもがん細胞が完全に消えたことを証明することはできない。そのため「完治」という表現はせず、腫瘍を検出できなくなった時点で「緩解(かんかい・寛解とも)[1]」したと表現する。これは、同じ血液のがんである白血病と同様の扱いである。緩解に至ってもがん細胞が残存していることがあって、再発・転移するケースもある。 →詳細は「転移」を参照
原因はわかっていないが、ウイルス説・カビ説・遺伝説などがある。小児白血病、絨毛癌などと並んで、悪性腫瘍の中では、比較的抗がん剤が効きやすいとされる。抗がん剤は活発な細胞を攻撃するため、一般に、がんの進行が早い悪性度の高いものほど抗がん剤に対する感受性が強く、進行の遅い低悪性度は感受性が低いとされている。 症状頸部(首)、鼠蹊部(股の付け根)、腋窩(腋の下)などのリンパ節が腫大する(腫れる)ことが多い。リンパ節が1cmを超え肥大が進行したり、腫瘤の数が短期間で増加する場合は、慢性リンパ節炎、結核性リンパ節炎、亜急性壊死性リンパ節炎などがある。また、腫脹の原因が不明な場合は一度感染したEBウイルスが再活性化、病症が慢性化していないか調べることも重要である。 各臓器に発生するリンパ腫の場合にはレントゲン撮影や内視鏡による検査で発見される場合もある。また全身の倦怠、発熱、盗汗(ねあせ)、体重の減少などがみられる場合もあり、これらの全身症状はB症状と呼ばれる。B症状は、予後不良因子とされている。
進行すると全身の衰弱、DIC(播種性血管内凝固症候群)、多臓器不全などから死に至る。 検査・診断 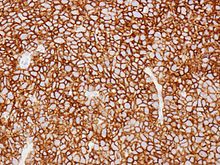 リンパ腫を疑う場合は触診、血液検査、造影CT検査などを行い病変の部位を検索するが、確定診断はリンパ節生検を行うことにより病理組織分類や遺伝子異常の検索もおこなうことがある。針生検での診断は難しいため、リンパ節を切り取って組織を調べることが多い。 病期分類リンパ腫の病期分類としては、次のAnn Arbor分類が世界的に用いられている。通常の癌と異なり、0期という分類はない。
※造血器腫瘍診療ガイドライン[2]より引用し改変。 ほかに、Lugano 分類が使用される事もある。
※造血器腫瘍診療ガイドライン[2]より引用し改変。 予後因子国際予後因子 (international prognosis index: IPI) が有名である。予後因子の数で患者を層別化し、予後を判定する。予後因子として、 が挙げられている。標準治療(CHOP療法など)を行った場合の予後は、5年生存率が25%程度。 組織学的分類非ホジキンリンパ腫は、ホジキンリンパ腫に該当しない多様なリンパ系組織のがんの総称であるので、世界的に統一された分類というのはなかったが、1999年に発表されたWHO分類が現在有効である。非ホジキンリンパ腫は、B細胞ががん化するか、T細胞あるいはNK細胞ががん化するかによって大きく2つに分類される。前者をB細胞性腫瘍と言い、後者をT/NK細胞性腫瘍と言う。 WHO分類リンパ球の腫瘍としては急性リンパ性白血病 (ALL)、慢性リンパ性白血病 (CLL)、悪性リンパ腫、多発性骨髄腫を始め各種ある。それぞれ、正常リンパ球のどの段階で発癌したかによって性質が異なると考えられている。そのためリンパ球の成熟過程を知っておくことが理解の助けとなる。 学問的には急性白血病という概念などなくして骨髄球性疾患とリンパ球性疾患に分けたほうがすっきりする。しかし、ALLは臨床経過が急性骨髄性白血病 (AML) に非常に近く、そのような単純な分類は臨床家が受け入れることができない。急性と慢性の違いに関しても、骨髄性とリンパ性とは随分印象が異なる。AMLと慢性骨髄性白血病 (CML) は確かに鑑別が重要だが、ALLとCLLは鑑別することはまずない。教科書で急性白血病と慢性白血病の違いは分化障害の有無とかといった項目が並ぶが、これは骨髄性のみ気にするべき事項であってリンパ性では問題にならない。CMLは原発性骨髄線維症や本態性血小板血症といった骨髄増殖性疾患に分類され、さらにAMLとなる「急性転化」があるので区別が重要となる。 二次性白血病としてはMDS、アルキル化薬によるものも知られている。また白血化という言葉があるが、これは末梢血に腫瘍細胞が見られることで、急性白血病ならば芽球、リンパ腫ならば異型リンパ球やOtherでカウントされることが多い。これらは自動測定機では見逃すことが多いので、鏡検する必要がある。 B細胞の成熟Bリンパ球の幹細胞は骨髄に存在する。ここでVDJ領域の再構成を行いIgMを発現し成熟B細胞となる。骨髄内の抗原と反応してしまうB細胞はこの時点でアポトーシスされる。成熟B細胞は骨髄を離れてリンパ組織へ行く。リンパ組織では各種相互作用に応じて分化する。T細胞非依存抗原と相互作用できた場合はIgM産出細胞(形質細胞、一部B細胞)となり、T細胞依存性抗原としか相互作用ができないと胚中心に移行し、クラススイッチを起こし、IgG産出細胞となる。これで形質細胞または記憶B細胞になる。クラススイッチを起こした形質細胞は短命のものと長命のものに分かれる。短命のものはリンパ組織内に留まり、長命のものは前駆形質細胞となり骨髄循環に適応し、抗体を産出しつづける。これらのどの段階で発癌したかによって腫瘍の性質が異なるのではないかというのが近年の考え方である。幸いなことにこれらの分化成熟過程における抗原の変化はよく知られている。多発性骨髄腫で形質細胞が骨髄に留まるのが不思議だが、長命の形質細胞は骨髄循環に適応しているので、骨髄で増殖してもおかしくない。M蛋白血症を起こすもののうち、IgM産生場合だけ特に問題ないのもIgM分泌は分化過程が違うということで多少は説明できる。しかしなぜ予後まで違うのかは、今のところ説明できない。 T細胞の成熟T細胞はまず骨髄の造血幹細胞から生じる。リンパ球前駆細胞の状態で胸腺に達することで正の選択、負の選択をうけていく。胸腺皮質から胸腺髄質へいたる過程で成熟、また不適切なものはアポトーシスに導かれる。胸腺髄質に達することにはCD4系とCD8系に分かれる。成熟T細胞のマーカーとしてはTCRやCD3が知られている。 治療法治療法は抗がん剤化学療法、放射線療法、支持療法を単独で、もしくは組み合わせて行う。造血幹細胞移植を行うこともある。疾患毎に、病期や予後因子等によって推奨される治療法は異なるので、詳細は各疾患の治療の項目を参照されたい。 悪性リンパ腫による神経系障害悪性リンパ腫の神経系障害は圧迫、直接浸潤、遠隔効果によるものに大別される。圧迫によるものの代表例はリンパ腫の転移性硬膜外腫瘍による圧迫性脊髄症がよく知られている。直接浸潤は浸潤する部位により中枢神経系に浸潤する中枢神経リンパ腫症(CNS lymphoma)、末梢神経系に浸潤する神経リンパ腫症(neurolymphomatosis)、筋肉に浸潤する筋リンパ腫症(muscle lymphoma)に大別される。また免疫不全に伴う場合は免疫不全関連リンパ増殖性疾患(IDLPD)として区別される[4]。遠隔効果によるものは傍腫瘍性神経症候群である。 中枢神経系悪性リンパ腫による中枢神経系の障害には中枢神経リンパ腫症、腫瘤形成による圧迫、傍腫瘍性神経症候群がある。 中枢神経リンパ腫症中枢神経リンパ腫症には全身性リンパ腫の中枢神経系浸潤、中枢神経系原発リンパ腫(primary CNS lymphoma、PCNSL)、血管内リンパ腫症(intravascular lymphomatosis)に大別される。 全身性リンパ腫の中枢神経系浸潤全身性リンパ腫の中枢神経系浸潤の大半はびまん性大細胞型B細胞リンパ腫である。診断時より中枢神経系浸潤している場合と治療後に中枢神経系に再発する場合がある。浸潤様式に脳実質内腫瘤形成型と髄膜播種型と両者の合併が知られている。浸潤した部位によって麻痺や失語のような巣症状、認知機能低下や性格変化など非局在性症候や頭蓋内圧亢進症による頭痛、嘔気などが認められる。比較的高頻度にみられる症状は脳神経麻痺であり特に外眼筋麻痺と顔面神経麻痺が多い。全身性リンパ腫の中枢神経系の再発は5%と比較的稀である[5][6][7]。しかし予後は不良であり50%生存期間は6ヶ月であり、2年生存率は27%という報告もある[8]。治療は高用量メソトレキセートの全身投与が優れているが副作用も多い[9]。 その他ステロイドや抗がん剤の髄腔内投与や全脳放射線照射などが行われる。リツキシマブの髄腔内投与の報告もあるが一般的ではない[10][11]。 原発性中枢神経系リンパ腫眼球を含む中枢神経系に原発する中枢神経系に原発する悪性リンパ腫であり、中枢神経系以外には悪性リンパ腫が存在しないものである。病理学的には大多数がびまん性大細胞型B細胞リンパ腫である。臨床症状と画像所見が極めて多彩であり「すべての神経疾患の鑑別にサルコイドーシスと悪性リンパ腫を挙げよ」ともいわれる。原発性脳腫瘍の3.1%を占め、年間人口10万人あたり約0.5人が発症する[12]。免疫不全に伴い発症する原発性中枢神経系リンパ腫はEBウイルスの関与が示唆されている[4]が免疫能正常の患者の発生原因は不明である[13]。 全身性リンパ腫の中枢神経系浸潤と同様に脳実質内腫瘤形成型と髄膜播種型の浸潤様式があるが原発性中枢神経系リンパ腫で髄膜播種型のみを示すことは極めて稀である。この稀な病態をprimary leptomeningeal lymphomaという[14]。また特殊な病態としてlymphomatosis cerebriというものが知られている[15]。これは腫瘤を形成せず、びまん性に白質脳症が両側性に出現するという原発性中枢神経系リンパ腫の特殊系である。亜急性に進行する認知機能障害、性格変化、歩行時のふらつきといった非局在性の神経症状が中心である。lymphomatosis cerebriの予後は不良で治療をしても半年以内に死亡することが多い。 原発性中枢神経系リンパ腫は通常中枢神経系に限局し、他部位に浸潤、転移することは極めて稀である。複数回中枢神経系に再発しても全身転移は稀である。治療としては高用量MTXの全身投与などが行われ2年生存率が50~70%であり5年生存率が20~40%である[12]。 眼内悪性リンパ腫の多くは原発性中枢神経系リンパ腫の亜型である。ステロイド抵抗性のぶどう膜炎の際に鑑別にあがる。 原発性中枢神経系リンパ腫では髄液IL-10がよいマーカーになると報告されている[16]。 血管内リンパ腫症血管内リンパ腫症(intravascular lymphomatosis)は主に節外臓器の微小血管内を閉塞性に進展する悪性リンパ腫である。病理学的にはびまん性大細胞型B細胞細胞リンパ腫の亜型である。血管内リンパ腫症で血管腔の血管内皮に細胞が集まりやすい理由は、細胞の表面に発現される分子によると考えられている。血管内リンパ腫症は極めて稀であり、欧米では100万人あたり1人とされているがアジアでの頻度は不明である。皮膚症状や神経症状が主体のWestern variantと血球貪食症候群を合併するAsian variantが知られている[17][18]。一般に発症は亜急性で経過は急速進行性であり、約6ヶ月~2年の経過で多臓器不全により死亡し、病理解剖で確定診断されることが多かった。しかしランダム皮膚生検など診断法の改善やCHOP療法とリツキシマブとの併用療法の普及により予後は改善してきている。筋生検による診断率も高い[19][20][21]。中枢神経系の障害を認める血管内リンパ腫で選択される治療法は確立していない。HD-MTXとR-CHOPを組み合わせた併用療法がしばしば行われる[22]。
神経症状(39%)と皮膚症状(39%)が主症状である[23]。典型的な皮疹は有痛性の発赤病変である。認知症や末梢神経障害など急激に進行する神経徴候を伴うことが多い。骨髄(32%)、脾臓(26%)、肝臓(26%)も障害されることが多い[24][25]。
神経症状(27%)、皮膚症状(15%)である。貧血(63%)、血小板減少(29%)、白血球減少(24%)や血球貪食症候群(59%)といった血球異常が認められる。骨髄(75%)、脾臓(67%)、肝臓(55%)も障害されることが多い。B症状も認められることが多い[26][27]。
皮膚に限局するタイプである。
血管内リンパ腫は不明熱、易疲労感などの全身症状、発疹、紅斑といった皮膚症状や認知機能障害や意識障害などの進行性の神経症状が認められる。
血管内リンパ腫は不明熱と多臓器不全を起こす疾患として知られており、特に不明熱とPS不良の症例で疑う。
血管内リンパ腫に認められる皮膚病変は多彩である。1999年にKrausらが外見上異常がない皮膚でも血管内リンパ腫の病変が認められることを報告している[28]。
血管内リンパ腫は全経過を通してみると60%以上で認められる[23]。最も多いのが脳血管障害(76%)であり、脊髄・神経根障害(38%)、亜急性脳症(27%)、脳神経障害(21%)、眼科的障害(16%)、末梢神経障害(5%)、ミオパチー(3%)である[29]。脳血管障害は脳梗塞が多く、亜急性脳症は意識障害や精神症状を示す。脊髄・神経根障害ではくも膜腔から脳実質内の小血管内腔に腫瘍細胞が充満し頸髄から腰髄まで広範囲にわたる虚血性の壊死病変を認める。好発部位は腰髄から仙髄であり対麻痺、感覚障害、膀胱直腸障害を示す。中枢神経由来の神経症状を症状別でみると認知機能低下(認知症か急性脳症)が61%、麻痺が22%、痙攣が13%であった[30]。認知機能低下が最も多いのが注目に値する。血管内リンパ腫による急速進行性認知症も多数報告されており、死亡例の報告が多い[31][32][33][34]が改善例[35][32]の報告もある。神経症状は小血管内腔に腫瘍細胞が充満した結果の虚血と考えられている[36][37]。血管内リンパ腫の頭部MRI所見としては橋のT2延長病変、非特異的白質病変、梗塞様病変、髄膜肥厚の4パターンが報告されている[38]。さらに腫瘤性病変も加えて5パターンとする報告もある[39]。MRIにおけるT2延長病変は虚血性病変と考えられている[40][41][42][43][44]が、治療によってMRI所見が改善する例もある[45][39]ため腫瘍による細胞密度の増加を示している可能性もある。また剖検例と比較するとMRIではすべての病変が検出できているわけではないと考えられる[46][39]。血管内リンパ腫では血清IL-10が高値になるという報告がある[47]。 中枢神経の傍腫瘍性神経症候群悪性リンパ腫の遠隔効果として辺縁系脳炎、亜急性小脳変性症、亜急性壊死性脊髄炎、スティッフパーソン症候群、オプソクローヌス・ミオクローヌス症候群、肉芽腫性脳血管炎が知られている[48]。 末梢神経系悪性リンパ腫による末梢神経系の障害には末梢神経リンパ腫症(neurolymphomatosis)、腫瘤形成による神経組織の圧迫、血管内リンパ腫による虚血性病変、遠隔効果による傍腫瘍性神経症候群が知られている。 末梢神経リンパ腫症末梢神経リンパ腫症(neurolymphomatosis)は悪性リンパ腫が末梢神経へ浸潤することである。末梢神経原発のものが狭義の末梢神経リンパ腫症であり、それ以外に全身性リンパ腫の末梢神経浸潤や全身性リンパ腫の治療後末梢神経再発などが考えられる。典型的には有痛性の多発神経障害や多発神経根障害が起こる。MRIやFDG-PETで評価する。 血管内リンパ腫症血管内リンパ腫症の末梢神経障害は多彩な表現型をとる。神経生検や筋生検で診断される例もある[49][50]。末梢神経由来の神経症状を症状別にみると筋力低下が60%で神経因性膀胱が37%であった[30]。神経伝導検査で末梢神経障害を認める例も少なからずあり、その機序は虚血に伴う軸索障害性の多発単神経叢障害とされるが[51]、オニオンバルブ形成を認めた症例もあり免疫介在性の機序も疑われる[52]。 末梢神経の傍腫瘍性神経症候群悪性リンパ腫の遠隔効果として亜急性感覚性ニューロノパチー、感覚性ニューロパチー、運動性ニューロパチー、感覚運動性ニューロパチー、CIDP、血管炎性ニューロパチー、神経ミオトニアが知られている。亜急性感覚性ニューロノパチーで血清にTrk抗体が認められる例もある。 筋肉悪性リンパ腫の筋肉の障害には末梢神経障害による神経原性筋萎縮、筋自体への浸潤である筋リンパ腫症(muscle lymphoma)、血管内リンパ腫の筋内血管病変、傍腫瘍性神経症候群の筋炎、骨髄穿刺に伴う殿筋血腫、感染症合併による筋膿瘍、アミロイドーシスによるミオパチー、同種移植後のGVHDとしての筋炎などがある。また神経筋接合部の傍腫瘍性神経症候群としては重症筋無力症とランバート・イートン症候群が知られている。 神経原性筋萎縮筋生検をしても筋内神経にリンパ腫細胞が認められることは稀である。 筋リンパ腫症筋リンパ腫症(muscle lymphoma)は悪性リンパ腫が筋肉へ浸潤することである。筋肉が原発の場合と全身性リンパ腫の筋肉浸潤が考えられる。通常、血清CK値は上昇しない。組織学的に筋周鞘血管周囲や筋内鞘にリンパ腫細胞が浸潤する。進行すれば筋を置換するような形になる。また再発による筋リンパ腫もある。 血管内リンパ腫症筋肉MRIで異常信号を呈した部位の筋生検で診断ができず、腎生検で血管内リンパ腫症と診断した例がある[53]。異常信号は神経原性筋萎縮と考えられる。筋肉しばしば血管内リンパ腫症の組織診が行われる[54][49][55]。筋原性変化の程度は報告により幅がある。血管外である筋細胞に浸潤する例も報告されている[56]。化学療法で筋力が回復した例もある[57][56]。 筋肉の傍腫瘍性神経症候群悪性リンパ腫を合併する筋炎や悪性リンパ腫を合併する重症筋無力症やランバート・イートン症候群が知られている。 悪性リンパ腫になった人物(アイウエオ順)
脚注出典
参考文献
関連項目
外部リンク
|
||||||||||||||||||||||||