|
Adrenalina
La adrenalina, también conocida como epinefrina por su Denominación Común Internacional (DCI), es una hormona y un neurotransmisor.[1] Es una sustancia cronotrópica positiva; aumenta la frecuencia cardíaca, contrae los vasos sanguíneos y dilata las vías respiratorias. Tradicionalmente se pensaba que la adrenalina participaba en la reacción de lucha o huida del sistema nervioso.[2] Hoy sabemos que la hormona responsable de esta reacción es la osteocalcina, sintetizada en los huesos. La vía de lucha o huida es distinta de otras mediadas por hormonas liberadas por las glándulas suprarrenales, como el cortisol, la adrenalina y la noradrenalina. Este hallazgo, publicado en 2019 en Cell Metabolism, ayuda a explicar por qué personas y animales que carecen de cortisol y moléculas adicionales producidas por las glándulas suprarrenales pueden aumentar la respuesta al estrés agudo. «La noción de que el hueso media la respuesta al estrés es totalmente nueva, al igual que la noción de que las glándulas suprarrenales no median la respuesta al estrés«, afirma Gerard Karsenty. “Esto verifica –añade- el concepto de que el hueso se creó en parte como herramienta para combatir el peligro agudo. Clínicamente, sugiere que respondemos mejor al estrés cuando somos jóvenes ya que tenemos una osteocalcina alta. Cuando somos mayores es mucho menor». Químicamente, la adrenalina es una catecolamina, una monoamina producida solo por las glándulas suprarrenales a partir de los aminoácidos fenilalanina y tirosina. La adrenalina es el neurotransmisor que se libera de la médula suprarrenal, en tanto que, de los ganglios paravertebrales se libera noradrenalina. El término adrenalina se deriva de las raíces latinas ad- y renes que literalmente significa "junto al riñón", en referencia a la ubicación anatómica de la glándula suprarrenal en el riñón. Las raíces griegas epi y nephros tienen un significado similar, "encima del riñón", y dan origen a epinefrina. El término epinefrina es usualmente abreviado a epi en la Jerga médica.[3] Los extractos suprarrenales que contienen adrenalina se obtuvieron por primera vez por el fisiólogo polaco Napoleon Cybulski en 1895. Estos extractos, que él llamó nadnerczyna, contenían epinefrina y otras catecolaminas.[4] El químico japonés Jokichi Takamine y su asistente Keizo Uenaka descubrieron independientemente la adrenalina en 1900.[5][6] En 1901, Takamine aisló y purificó con éxito la hormona de las glándulas suprarrenales de ovejas y bueyes.[7] La adrenalina fue por primera vez sintetizada en un laboratorio por Friedrich Stolz y Henry Drysdale Dakin, de forma independiente, en 1904.[6] Es una aminohormona. Aplicaciones médicas La epinefrina es usada para tratar una serie de afecciones como: paro cardiorrespiratorio, anafilaxia, y sangrado superficial.[8] Ha sido históricamente usada para tratar los broncoespasmos y la hipoglucemia, pero ahora se prefiere utilizar fármacos más selectivos, tales como el salbutamol y la dextrosa respectivamente. Paro cardíacoLa adrenalina se usa como medicamento para tratar el paro cardíaco y otras arritmias cardíacas que resulten en un gasto cardíaco disminuido o ausente. La acción de la adrenalina consiste en el incremento de la resistencia periférica mediante la vasoconstricción receptor α1-dependiente y el incremento del gasto cardíaco mediante su unión a los receptores β1. Las concentraciones ACLS habituales para las inyecciones son de 1:10.000. AnafilaxiaDebido a sus efectos de dilatación en la vía aérea, la adrenalina es el fármaco de elección para tratar la anafilaxia. También es útil en el tratamiento de la septicemia. Los pacientes con alergia a proteínas[9] sometidos a inmunoterapia pueden recibir un "enjuague" de adrenalina antes de que se administre el extracto alergénico, reduciendo así la respuesta del sistema inmune al alergénico administrado.[10] Debido a las diversas expresiones de receptores α1 o β2, dependiendo del paciente, la administración de adrenalina puede elevar o reducir la presión sanguínea, dependiendo de que el aumento o disminución neta de la resistencia periférica permita balancear los efectos inotrópicos y cronotrópicos positivos de la adrenalina en el corazón, efectos que respectivamente incrementan la contractilidad y la frecuencia cardíaca. Las concentraciones habituales para las inyecciones subcutáneas o intramusculares son de 1:1.000. Laringitis (crup)La epinefrina racémica ha sido históricamente usada para el tratamiento de la laringitis.[11][12] La epinefrina racémica es una mezcla 1:1 de los isómeros dextrógiro (D) y levógiro (L) de la epinefrina.[13] La forma L es el componente activo.[13] La epinefrina racémica funciona a través de la estimulación de los receptores adrenérgicos-α en las vías respiratorias resultando en la vasoconstricción de la mucosa y una disminución en los edemas subglóticos, y a través de la estimulación de los receptores adrenérgicos-β en la relajación del músculo liso bronquial.[12] En anestésicos localesLa epinefrina se añade a una serie de anestésicos locales inyectables, tales como la bupivacaína y lidocaína, como un vasoconstrictor que permite retardar la absorción y por lo tanto prolongar la acción del agente anestésico y potenciarlo. Algunos de los efectos adversos del uso de anestésicos locales, tales como la aprensión, taquicardia y temblores, podrían deberse a la acción de la epinefrina.[14] Autoinyectores La epinefrina está disponible en sistemas de autoadministración (autoinyectores). Estos dispositivos se presentan en dos formatos según su contenido de adrenalina: 0,15 mg (150 µg) y 0,3 mg (300 µg). El de 0,15 mg está destinado a niños de hasta 35 kg de peso, y los de 0,3 mg a niños de más peso, adolescentes y adultos. Están presentes en los mercados de cada país bajo distintas marcas comerciales. A efectos de monitorizar el estado de conservación de la epinefrina frente a una posible desnaturalización (por agresiones lumínicas, térmicas,...), los autoinyectores disponen de una ventana transparente que permite realizar la observación visual de la transparencia del líquido. Los usuarios de autoinyectores deben realizar la comprobación visual diariamente, así como reemplazarlos cada 18 meses (coincidiendo con el plazo de caducidad o vida útil del componente activo). EjercicioUn estímulo fisiológico para la secreción de adrenalina es el ejercicio. Esto se demostró por primera vez midiendo la dilatación de una pupila (desnervada) de un gato en una cinta de correr,[15] posteriormente confirmado mediante un ensayo biológico en muestras de orina.[16] Los métodos bioquímicos para medir las catecolaminas en plasma se publicaron a partir de 1950.[17] Aunque se han publicado muchos trabajos valiosos utilizando ensayos fluorimétricos para medir las concentraciones totales de catecolaminas, el método es demasiado inespecífico e insensible para determinar con precisión las cantidades muy pequeñas de adrenalina en el plasma. El desarrollo de métodos de extracción y ensayos radioenzimáticos derivados de isótopos enzimáticos (REA) transformó el análisis a una sensibilidad de 1 pg para la adrenalina.[18] Los primeros ensayos de plasma REA indicaron que la adrenalina y las catecolaminas totales aumentan al final del ejercicio, principalmente cuando comienza el metabolismo anaeróbico.[19][20][21] Durante el ejercicio, la concentración de adrenalina en sangre aumenta en parte por el aumento de la secreción de la médula suprarrenal y en parte por la disminución del metabolismo de la adrenalina debido a la reducción del flujo sanguíneo al hígado.[22] La infusión de adrenalina para reproducir las concentraciones circulantes de adrenalina en el ejercicio en sujetos en reposo tiene poco efecto hemodinámico, aparte de una pequeña caída de la presión arterial diastólica mediada por β 2.[23][24] La infusión de adrenalina dentro del rango fisiológico suprime la hiperreactividad de las vías respiratorias humanas lo suficiente como para antagonizar los efectos constrictores de la histamina inhalada.[25] Un vínculo entre el sistema nervioso simpático y los pulmones se demostró en 1887 cuando Grossman demostró que la estimulación de los nervios del acelerador cardíaco revertía la constricción de las vías respiratorias inducida por la muscarina.[26] En experimentos con perros, en los que se cortaba la cadena simpática al nivel del diafragma, Jackson mostró que no había inervación simpática directa del pulmón, pero que la broncoconstricción se revertía mediante la liberación de adrenalina de la médula suprarrenal.[27] No se ha informado una mayor incidencia de asma en pacientes adrenalectomizados; aquellos con predisposición al asma tendrán cierta protección contra la hiperreactividad de las vías respiratorias de su terapia de reemplazo de corticosteroides. El ejercicio induce una dilatación progresiva de las vías respiratorias en sujetos normales que se correlaciona con la carga de trabajo y no se evita con el bloqueo beta.[28] La dilatación progresiva de las vías respiratorias con el aumento del ejercicio está mediada por una reducción progresiva del tono vagal en reposo. El bloqueo beta con propranolol provoca un rebote en la resistencia de las vías respiratorias después del ejercicio en sujetos normales durante el mismo curso de tiempo que la broncoconstricción observada con el asma inducida por el ejercicio.[29] La reducción de la resistencia de las vías respiratorias durante el ejercicio reduce el trabajo respiratorio. Efectos adversosPosibles reacciones adversas a la epinefrina son: palpitaciones, taquicardias, arritmias cardíacas, ansiedad, cefaleas, temblores, hipertensión, y edema pulmonar agudo.[30] Su uso está contraindicado en pacientes en tratamiento con β-bloqueadores no-selectivos, debido a que la interacción podría resultar en una hipertensión severa e incluso en una hemorragia cerebral.[31] Aunque comúnmente se cree que la administración de epinefrina puede causar un fallo cardiaco por estrechar las arterias coronarias, este no es el caso. Las arterias coronarias tienen solamente receptores β2, que provocan una vasodilatación en presencia de epinefrina.[32] Sin embargo, no está probado definitivamente que la administración de dosis altas de epinefrina mejore la supervivencia o la incidencia de secuelas neurológicas en víctimas adultas de un paro cardíaco.[33] Medición en fluidos biológicosLa epinefrina puede ser cuantificada en la sangre, plasma o suero como ayuda diagnóstica para monitorear la administración terapéutica o para identificar el agente causante en una posible víctima de envenenamiento. Las concentraciones de epinefrina endógena en el plasma en un adulto en reposo son normalmente menores de 10 ng/L, pero pueden subir 10 veces durante el ejercicio y 50 veces o más durante periodos de estrés. Los pacientes con feocromocitoma tienen normalmente niveles de epinefrina en el plasma de 1.000-10.000 ng/L. La administración parenteral de epinefrina para el cuidado intensivo en pacientes con afecciones cardiacas puede llevar a concentraciones de 10.000 a 100.000 ng/L.[34][35] Mecanismo de acciónVéase también: Receptor adrenérgico
Como hormona, la epinefrina actúa en casi todos los tejidos del cuerpo. Sus acciones varían según el tipo de tejido y la expresión de los distintos receptores adrenérgicos en cada tejido. Por ejemplo, la epinefrina causa la relajación del músculo liso en las vías respiratorias pero causa contracciones en el músculo liso de las arteriolas. La epinefrina actúa uniéndose varios receptores adrenérgicos. La adrenalina es un agonista no selectivo de todos los receptores adrenérgicos, incluyendo los receptores α1, α2, β1, β2, y β3.[31] La unión de la epinefrina a estos receptores origina una serie de cambios metabólicos. La unión con los receptores adrenérgicos α inhibe la secreción de insulina en el páncreas; estimula la glucogenólisis en el hígado y el músculo; y estimula la glucólisis en el músculo.[36] La unión con los receptores adrenérgicos β provoca la secreción de glucagón en el páncreas, acrecienta la secreción de la hormona adrenocorticotropa (ACTH) en la glándula pituitaria e incrementa la lipólisis en el tejido adiposo. Juntos, estos efectos llevan a un incremento de la glucemia y de la concentración de ácidos grasos en la sangre, proporcionando sustratos para la producción de energía dentro de las células de todo el cuerpo.[36] La adrenalina es el activador más potente de los receptores α, es 2 a 10 veces más activa que la noradrenalina y más de 100 veces más potente que el isoproterenol. Además de los cambios metabólicos, la epinefrina también lleva a amplias interacciones a través de todos los sistemas de órganos.
Biosíntesis y regulaciónLa adrenalina es sintetizada en la médula de la glándula suprarrenal en una ruta enzimática que convierte el aminoácido tirosina en una serie de intermediarios y, finalmente, en adrenalina. La tirosina es primero oxidada para obtener levodopa, que posteriormente se descarboxila para dar dopamina. La oxidación de esta molécula proporciona norepinefrina que luego es metilada para dar epinefrina. La adrenalina también es sintetizada al metilarse la amina distal primaria de la norepinefrina por la acción de la enzima feniletanolamina N-metiltransferasa (PNMT) en el citosol de las neuronas adrenérgicas y células de la médula adrenal (llamadas células cromafínicas). La PNMT solo se encuentra en el citosol de las células de la médula suprarrenal. La PNMT usa la S-adenosilmetionina como cofactor para donar el grupo metilo a la norepinefrina, creando adrenalina. 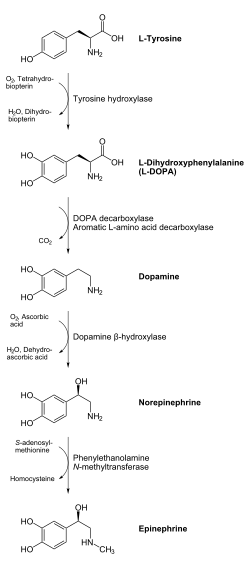 Para que la norepinefrina sirva como sustrato de la PNM en el citosol, primero debe ser trasladada fuera de los gránulos de las células cromafínicas a través del intercambiador catecolaminas-H+ VMAT1. El VMAT1 también es responsable de transportar la recién sintetizada adrenalina de vuelta del citosol a los gránulos de las células cromafínicas, desde donde es liberada fuera de la célula. En las células hepáticas, la adrenalina se une al receptor adrenérgico β, que cambia de conformación y ayuda a las G, un tipo de proteína G, a transformar el GDP en GTP. Esta proteína G trimérica se disocia en subunidades alfa y beta/gamma. Las G alfa se unen a la adenilciclasa, convirtiendo el ATP en AMP cíclico. El AMP cíclico se une a una subunidad reguladora de la proteína quinasa A y la proteína quinasa A fosforila la fosforilasa quinasa. Mientras tanto, las G beta/gamma se unen al canal de calcio, lo que permite la entrada de los iones de calcio al citoplasma. Los iones de calcio se unen a las proteínas calmodulinas, una proteína presente en todas las células eucariotas, que luego se unen a la fosforilasa quinasa y completan su activación. La fosforilasa quinasa fosforila la glucógeno fosforilasa, que luego fosforila el glucógeno y lo convierte en glucosa-6-fosfato. RegulaciónLos principales desencadenantes fisiológicos de la liberación de adrenalina son las tensiones, tales como las amenazas físicas, las emociones intensas, los ruidos, las luces brillantes y la alta temperatura ambiental. Todos estos estímulos se procesan en el sistema nervioso central.[37] La hormona adrenocorticotropa (ACTH) y el sistema nervioso simpático estimulan la síntesis de los precursores de adrenalina al incrementar la actividad de la tirosina hidroxilasa y dopamina beta-hidroxilasa, dos enzimas claves involucradas en la síntesis de catecolaminas. La ACTH también estimula a la corteza suprarrenal para que libere cortisol, lo que incrementa la expresión de PNMT en las células cromafínicas, intensificando la síntesis de adrenalina. Esto se hace con frecuencia en respuesta al estrés. El sistema nervioso simpático, actuando a través de los nervios esplácnicos que llegan a la médula suprarrenal, estimula la liberación de adrenalina. La acetilcolina liberada por las fibras simpáticas preganglionares de estos nervios actúan en los receptores nicotínicos, causando la despolarización celular y una entrada de calcio a través de los canales de calcio voltaje-dependientes. El calcio provoca la exocitosis de los gránulos cromafínicos y así libera la adrenalina (y noradrenalina) hacia el torrente sanguíneo. La adrenalina (como también la noradrenalina) ejerce una retroalimentación negativa para regular a la baja su propia síntesis en los receptores presinápticos adrenérgicos α2. Niveles anormalmente altos de adrenalina pueden provocar una variedad de afecciones, tales como el feocromocitoma y otros tumores de los ganglios simpáticos. Su acción finaliza con su recaptación en las terminaciones nerviosas, la dilución y la degradación metabólica por monoamino oxidasas y catecol-O-metil transferasas. Síntesis químicaLa epinefrina puede sintetizarse mediante la reacción de catecol con cloruro de cloroacetilo, seguido por la adición de metilamina para obtener la cetona, que se reduce al compuesto deseado. La mezcla racémica puede separarse usando ácido tartárico. La adrenalina natural es el esteroisómero (R)-(-)-L-adrenalina.  Para el aislamiento desde las glándulas suprarrenales de animales (inglés):
Producción sintética (inglés):
EtimologíaAunque fuera de los Estados Unidos se nombra de manera habitual como adrenalina, el USAN y la Denominación Común Internacional (DCI) para este fármaco es epinefrina porque adrenaline se parece demasiado a la marca adrenalin (sin la e final) comercializada por Parke, Davis & Co., la cual se encuentra registrada en los Estados Unidos. Véase también
Referencias
Bibliografía
Enlaces externos
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

