|
PoloacetalPoloacetal nebo poloketal je chemická sloučenina, která vzniká adicí alkoholu na aldehyd nebo keton. Předpona polo- naznačuje, že došlo k adici pouze jedné molekuly; acetaly a ketaly vznikají obdobně, adicí dvou molekul alkoholu.[1] Vznik a obecný vzorec Obecný vzorec poloacetalu je R1R2C(OH)OR, kde R1 a nebo R2 je často vodík a R (skupina navázaná na O) není vodík.
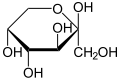
Cyklické poloacetaly a poloketalyPoloacetaly a poloketaly jsou obecně nestabilní sloučeniny. Cyklické poloacetaly, nazývané laktoly[2], jsou však v některých případech stabilní a dají se snadno připravit, obzvláště obsahují-li jejich molekuly pětičlenné nebo šestičlenné cykly. Tyto látky vznikají vnitromolekulární vzájemnou reakcí hydroxylové a karbonylové skupiny. Glukóza a mnoho dalších aldóz se vyskytuje v podobě cyklických poloacetalů, zatímco fruktóza (a podobné ketózy) vytváří cyklické poloketaly.
PřípravaPoloacetaly se připravují několika způsoby:
ReakcePoloacetaly a poloketaly lze považovat za meziprodukty při reakci alkoholů s aldehydy nebo ketony, kde je konečným produktem acetal či ketal:
Poloacetal může v kyselém prostředí reagovat s alkoholem za vzniku acetalu a může se rozkládat na aldehyd a alkohol. Aldehydy rozpuštěné ve vodě se vyskytují v rovnováze se svými hydráty (které jsou přítomny v mnohem menších koncentracích); obecný vzorec takového hydrátu je R-CH(OH)2. Obdobně se při přidání přebytku alkoholu budou v roztoku nacházet aldehyd, jeho poloacetal a acetal. Poloacetal vzniká díky nukleofilnímu ataku hydroxylové skupiny alkoholu na uhlík vazby C=O; acetaly jsou produkty substitučních reakcí katalyzovaných kyselinami. Přítomnost kyseliny umožňuje substituci hydroxylové skupiny alkoxylovou (-OR) skupinou. Přeměna poloacetalu na acetal je SN1 reakce. Tvorba poloketalů a ketalů z ketonů neprobíhá tak snadno jako u poloacetalů a acetalů. Ke zvýšení výtěžnosti reakce je při přípravě acetalů i ketalů potřeba odstraňovat vznikající vodu. ReferenceV tomto článku byl použit překlad textu z článku Hemiacetal na anglické Wikipedii.
Externí odkazy
|