|
Grafit
El grafit és un mineral de la classe dels elementals, i en la seua composició concreta intervé un element semimetàl·lic. Està format quasi exclusivament per àtoms de carboni, i es tracta de fet d'una de les formes al·lotròpiques en què es pot presentar el carboni elemental, juntament amb el diamant, el ful·lerè i altres, com el grafè. El grafit és la forma més estable del carboni en condicions estàndard (o a pressions i temperatures baixes), motiu pel qual se l'utilitza en termoquímica per a definir l'estat estàndard respecte del qual es mesura la calor de formació dels compostos del carboni. També és polimorf de la chaoïta i la lonsdaleïta. Rep el seu nom per Abraham Gottlob Werner l'any 1789, i el terme grafit deriva del grec γραφειν (graphein) que significa escriure. Es pot considerar el grafit com el carbó de màxim contingut en carboni, trobant-se per damunt de l'antracita, de manera que se'l pot anomenar meta-antracita, encara que normalment no se l'empra com a combustible degut al fet que és molt difícil encendre'l. També és possible entendre el grafit com una successió de capes de grafè superposades. Antigament, es va anomenar "molibundasna" (que no s'ha de confondre amb el mineral molibdenita).[1] Característiques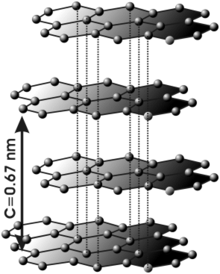 El grafit és de color negre amb lluentor metàl·lica, refractari i s'exfolia amb facilitat. En la direcció perpendicular a les capes presenta una conductivitat de l'electricitat baixa i que augmenta amb la temperatura, comportant-se doncs com un semiconductor. Al llarg de les capes la conductivitat és major i augmenta proporcionalment a la temperatura, comportant-se com un conductor semimetàl·lic. A diferència del diamant, encara que els dos estan formats per carboni, el grafit és molt tou i el diamant és el mineral més dur segons l'escala de Mohs. En el grafit els àtoms de carboni presenten hibridació sp2, això significa que forma tres enllaços covalents en el mateix pla a un angle de 120° (estructura hexagonal) i que un orbital Π perpendicular a aquest pla quedi lliure (aquests orbitals deslocalitzats són fonamentals per definir el comportament elèctric del grafit). L'enllaç covalent entre els àtoms d'una capa és extremadament fort, en canvi les unions entre les diferents capes es realitzen per forces de Van der Waals i les interaccions entre els orbitals Π, i són molt més febles. L'estructura laminar del grafit fa que sigui un material marcadament anisòtrop. El grafit té funcions de ratllar altres minerals per a mesurar la seva duresa, ja que no és gaire fràgil. De manera artificial, el grafit es pot convertir en diamant augmentant la temperatura i la pressió, i utilitzant un catalitzador per augmentar la velocitat de la reacció. El grafit és polimorf del diamant, la chaoïta i la lonsdaleïta. Té dos politips, el grafit-2H, que també cristal·litza en el sistema hexagonal, i el grafit-3R, que ho fa en el trigonal.[2][3] A més es coneixen dues varietats: la cliftonita, un grafit octaèdric pseudomòrfic després de kamacita, trobat en uns pocs meteorits de ferro, i el grafit urànic, un grafit que com el seu nom indica conté urani. Les condicions de pressió i temperatura dequilibri per a una transició entre grafit i diamant estan ben establertes teòricament i experimentalment. La pressió canvia linealment entre 1,7 GPa a 0 K i 12 GPa a 5.000 K (el punt triple del diamant/grafit/líquid).[4][5] Tot i això, les fases tenen una àmplia regió al voltant d'aquesta línia on poden coexistir. En temperatura i pressió normals, 20 °C (293 K) i 1 atmosfera estàndard (0.10 MPa), la fase estable del carboni és el grafit, però el diamant és metaestable i la seva taxa de conversió a grafit és menyspreable.[6] No obstant això, a temperatures superiors a aproximadament 4.500 K, el diamant es converteix ràpidament en grafit. La ràpida conversió de grafit en diamant requereix pressions molt per sobre de la línia d'equilibri: a 2.000 K, cal una pressió de 35 GPa.[4] FormacióEl grafit es troba en roques metamòrfiques com a resultat de la reducció de compostos de carboni sedimentàris durant el metamorfisme. També es troba en roques ígnies i en els meteorits.[7] Els minerals associats amb el grafit inclouen quars, calcita, diferents miques i turmalina. En meteorits s'ha trobat amb troilita i minerals silicats.[8] Els cristalls de grafit petits en ferro meteorític es coneixen com a cliftonita.[9] Alguns grans microscòpics tenen composicions de isòtops distintives, la qual cosa indica que es van formar abans del Sistema Solar.[10] Són un dels prop de 12 tipus de minerals coneguts que són anteriors al Sistema Solar i que també s'han detectat a núvols moleculars. Aquests minerals es van formar en els materials ejectats quan les supernoves van explotar o les estrelles de mida baixa o intermedi van expulsar els seus embolcalls exteriors al final de la seva vida. El grafit pot ésser el segon o tercer mineral més antic de l'Univers.[11][12] Encara que es pot produir artificialment, a partir de carboni amorf, hi ha molts jaciments naturals d'aquest mineral. Es troba en roques metamòrfiques, en què els processos associats amb la seva formació han transformat el carboni present en la matèria orgànica que contenia la roca original. Els principals països exportadors de grafit extret són, per ordre de major a menor tonatge: la Xina, Moçambic, Madagascar, Corea del Sud, Rússia, Canadà, Noruega i l'Índia.[13] Síntesi artificial del grafitEl 1893, Charles Street de Le Carbone va descobrir un procés per fabricar grafit artificial. A mitjan dècada de 1890, Edward Goodrich Acheson (1856-1931) va inventar accidentalment una altra forma de produir grafit sintètic després de sintetitzar carborund (carbur de silici o SiC). Va descobrir a diferència del carboni pur, produïa grafit gairebé pur. En estudiar els efectes de les altes temperatures en el carborund, va descobrir que el silici es vaporitza a uns 4.150°C (7.500°F), deixant el carboni en grafit. Aquest grafit es va fer valuós com a lubricant.[9] La tècnica d'Acheson per produir carbur de silici i grafit rep el nom de procés Acheson. El 1896, Acheson va rebre una patent pel seu mètode per sintetitzar grafit,[14] i el 1897 va començar la producció comercial.[9] El 1899 es va formar l'Acheson Graphite Co. El grafit sintètic també es pot preparar a partir de la poliimida i es comercialitza així.[15][16] Compostos d'intercalació de grafitDiferents molècules o ions poden penetrar a les capes del grafit. Per exemple, el potassi pot cedir un electró al grafit, quedant l'ió de potassi entre les capes. Aquest electró contribueix a augmentar la conductivitat que presentava el carboni. Es poden preparar diferents compostos d'intercalació amb diferents estequiometries i diferents espècies. En alguns casos la conductivitat resultant és més gran, com en el cas del potassi, i és el que passa generalment, però en altres, com per exemple amb fluor, és en menor mesura. Altres formes relacionadesHi ha altres formes anomenades de carbó amorf que tenen una estructura relacionada amb la del grafit:
Usos
LlapisLa possibilitat de deixar marques en el paper i altres objectes donen el seu nom al grafit. El grafit del llapis, o plom negre, és més comunament una barreja de pols de grafit i argila; va ser inventat per Nicolas-Jacques Conté el 1795.[17] Plumbago és un terme més antic per al grafit natural utilitzat per dibuixar, tradicionalment com un tros de mineral sense l'embolcall de fusta. Avui en dia, els llapis són encara un mercat petit però significatiu per al grafit natural. Al voltant del 7% dels 1,1 milions de tones produïdes en 2011 es va emprar per fer llapis.[18] Referències
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||