|
Enllaç carboni-carboniEls compostos d'organocarboni (o compostos orgànics del carboni) són compostos químics que contenen un enllaç químic entre carboni (C) i carboni (C) (enllaç C-C).[1] La química de l'organocarboni és la ciència corresponent que explora les propietats, l'estructura i la reactivitat d'aquests compostos. La forma més comuna és l'enllaç simple: un enllaç format per dos electrons, un de cadascun dels dos àtoms. L'enllaç únic carboni-carboni és un enllaç sigma i es forma entre un orbital hibridat de cadascun dels àtoms de carboni. A l'età, els orbitals són orbitals hibridats amb sp3, però també es produeixen enllaços simples formats entre àtoms de carboni amb altres hibridacions (per exemple, sp2 a sp2). De fet, els àtoms de carboni de l'enllaç senzill no necessiten ser de la mateixa hibridació. Els àtoms de carboni també poden formar enllaços dobles en compostos anomenats alquens o enllaços triples en compostos anomenats alquins. Es forma un doble enllaç amb un orbital hibridat sp2 i un orbital p que no està implicat en la hibridació. Es forma un enllaç triple amb un orbital sp hibridat i dos orbitals p de cada àtom. L'ús dels orbitals p forma un enllaç pi. Cadenes i ramificacionsEl carboni és un dels pocs elements que pot formar llargues cadenes dels seus propis àtoms, una propietat anomenada catenació. Això unit a la força de l'enllaç carboni-carboni dona lloc a un nombre enorme de formes moleculars, moltes de les quals són elements estructurals importants de la vida, de manera que els compostos de carboni tenen el seu propi camp d'estudi: la química orgànica.
La ramificació també és freqüent en els esquelets C−C. Els àtoms de carboni d'una molècula es classifiquen segons el nombre de veïns de carboni que tenen:[2][3]
En les «molècules orgàniques estructuralment complexes», és l'orientació tridimensional dels enllaços carboni-carboni en els llocs quaternaris la que dicta la forma de la molècula. A més, els loci quaternaris es troben en moltes molècules petites biològicament actives, com la cortisona i la morfina.[4] SíntesiLes reaccions de formació d'enllaç carboni-carboni són reaccions orgàniques en les quals es forma un nou enllaç carboni-carboni. Són importants en la producció de molts productes químics artificials com ara productes farmacèutics i plàstics. Alguns exemples de reaccions que formen enllaços carboni-carboni són les reaccions aldòliques, les reaccions de Diels-Alder, l'addició d'un reactiu de Grignard a un grup carbonil, una reacció de Heck, una reacció de Michael i una reacció de Wittig. La síntesi dirigida de les estructures tridimensionals desitjades per a carbonis terciaris es va resoldre en gran manera a finals del segle xx, però la mateixa capacitat per dirigir la síntesi de carboni quaternari no va començar a sorgir fins a la primera dècada del segle xxi.[4] Força i longitud d'enllaçL'enllaç senzill carboni-carboni és més feble que els enllaços C-H, O-H, N-H, H-H, H-Cl, C-F i molts enllaços dobles o triples, i és comparable en força als enllaços C-O, Si-O, P-O i SH,[5] però habitualment és considerat com a fort.
Els valors indicats anteriorment representen energies de dissociació d'enllaços C-C que es troben habitualment; ocasionalment, els valors atípics poden desviar-se dràsticament d'aquest rang.
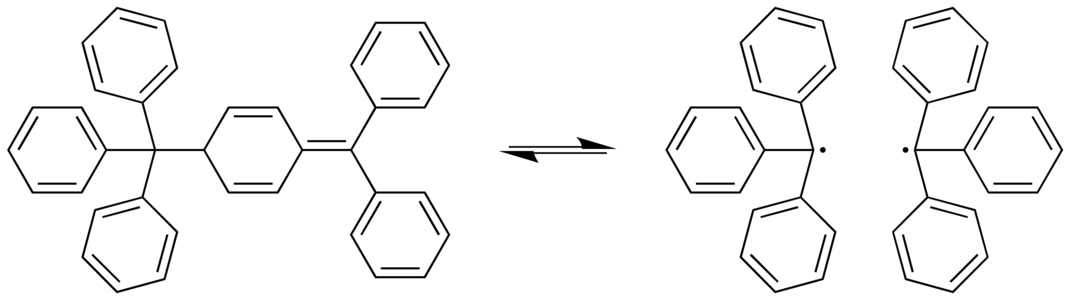
Casos extremsEnllaços senzill C-C, llargs i feblesS'han identificat diversos casos extrems on l'enllaç C-C és allargat. En el dímer de Gomberg, un enllaç C-C és bastant llarg (159,7 picòmetres). Aquest enllaç és el que es trenca de manera reversible i ràpida a temperatura ambient en solució.[6]
A la molècula encara més congestionada hexakis(3,5-di-tert-butilfenil)età, l'energia de dissociació de l'enllaç per formar el radical triarilmetil estabilitzat és només de 8 kcal/mol. També com a conseqüència de la seva severa congestió estèrica, l'hexakis(3,5-di-tert-butilfenil)etaà té un enllaç central molt allargat amb una longitud de 167 pm.[7] Dobles enllaços C=C, retorçats i feblesL'estructura del tetrakis(dimetilamino)etilè (TDAE) està molt distorsionada. L'angle díedre dels dos extrems N₂C és de 28º encara que la distància C=C és normal de 135 pm. El tetraisopropiletilè gairebé isoestructural també té una distància C=C de 135 pm, però el seu nucli C₆ és pla.[8] Enllaços triples C≡C, curts i fortsA l'extrem oposat, l'enllaç senzill carboni-carboni central del diacetilè és molt fort (160 kcal/mol), ja que l'enllaç senzill uneix dos carbonis d'hibridació sp. Els enllaços múltiples carboni-carboni són generalment més forts; s'ha determinat que el doble enllaç de l'etilè i el triple enllaç de l'acetilè tenen energies de dissociació d'enllaç de 174 i 230 kcal/mol, respectivament.[9] S'ha observat un triple enllaç molt curt de 115 pm per a les espècies d'iodini [HC≡C–I+Ph][CF₃SO₃–], a causa de la part de iodoni fortament extreta d'electrons.[10] Referències
Bibliografia
|